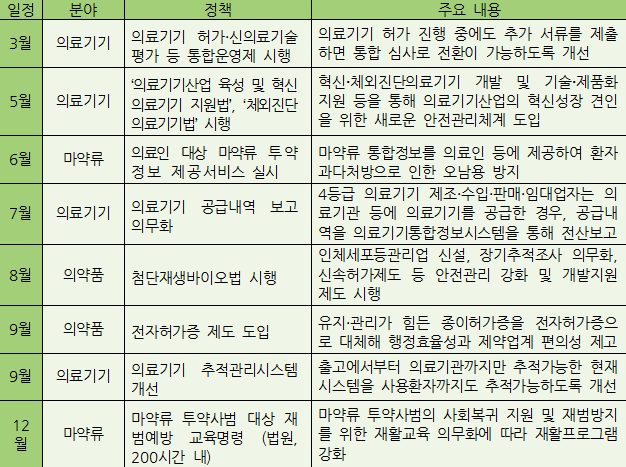
식품의약품안전처가 2020년에 달라지는 의약품과 의료기기 안전정책을 발표했다.
이에 따르면 내년 3월에 의료기기 허가 및 신의료기술평가 통합심사 전환제가 시행된다.
의료기기 허가·신의료기술평가 통합심사 제도를 활성화하기 위해 허가심사 진행 중에 추가로 서류를 제출하면 통합심사로 전환할 수 있다.
예컨대 허가와 요양급여, 신의료기술평가 신청시 구비서류를 갖추던 예전과 달리 동시 신청하든 허가 신청 후 통합운영하든 모두 가능하다.
이어 5월에는 의료기기산업 육성 및 혁신의료기기 지원법, 체외진단의료기기법이 시행된다.
6월에는 마약류 통합정보제공 서비스, 7월에는 의료기기 공급내역 의무보고 통합정보시스템이 도입된다.
8월에는 세포채취 부터 사용까지 안전 관리하고 치료기회 확대를 위한 첨단재생바이오법, 9월에는 의료기기 추적관리시스템과 의약품 등 전자허가증이 도입된다.
이어 12월에는 마약류 투약사범의 재범 예방 및 사회 복귀 지원 재활프로그램이 강화된다.