암젠코리아의 이베니티주 프리필드시린지(성분명: 로모소주맙)가 지난달 31일 식품의약품안전처 승인을 받았다.
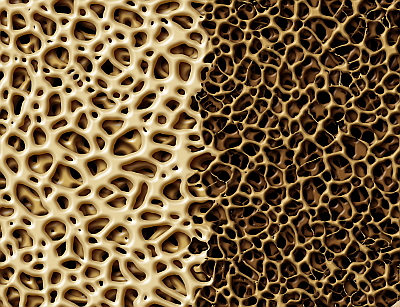
적응증은 골절 위험이 높은 폐경 후 여성 골다공증 환자의 치료와 골절 위험이 높은 남성 골다공증 환자의 골밀도 증가다.
이베니티는 골형성을 저해하는 단백질 스클레로스틴을 억제해 골형성을 높이고, 골흡수는 억제하는 이중효과를 갖고 있다.
투여법은 한 달에 한 번, 총 210mg 용량을 두 번에 나누어 각각 다른 투여 부위에 105mg 씩 연속 2번 피하 주사한다. 총 12회 투여하며 그 이후에는 골흡수 억제제를 통한 유지요법이 필요하다.
이번 승인은 3상 임상시험 FRAME과 ARCH BRIDGE의 결과에 근거했다. 폐경여성을 대상으로 한 FRAME에 따르면 이베니티는 전고관절 또는 대퇴골 경부 골밀도 T 스코어가 -2.5~-3.5인 환자의 척추 골절 위험이 투약 1년 차에 위약군 대비 73% 줄었다.
역시 골다공증과 취약성있는 골절을 가진 폐경여성을 대상으로 한 ARCH에서도 기존 골다공증치료제 알렌드로네이트에 비해 투약 2년째 척추골절위험이 50%, 33개월째에는 27% 낮았다.
남성 골다공증 환자를 대상으로 진행된 BRIDGE 임상에서는 투약 12개월째 요추 골밀도가 위약 대비 12.1% 증가했다.
관련기사
