가슴열지 않고 시술해 환자 부담 적어
개당 3~4천만원 외산품에 비해 저렴
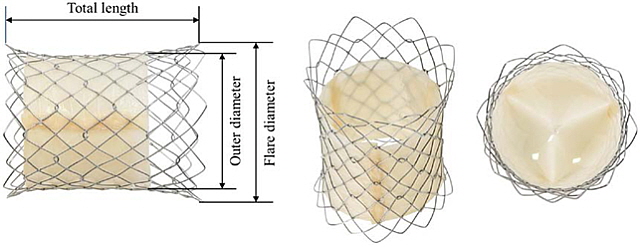
서울대병원이 개발한 인공심장판막이 식품의약품안전처의 허가를 받았다.
서울대병원은 지난 2004년에 태웅메디칼과 함께 보건복지부 지원 바이오이종장기사업단을 통해 폐동맥인공심장판막 개발에 들어갔다. 동시에 피부를 통해 간단하게 판막을 이식하는 스텐트 개발도 동시에 진행했다.
동물실험 이후 2016년부터 시작한 임상시험에서 환자 10명에게 이식하고 6개월을 추적 관찰한 결과 효과와 안전성이 입증됐다.
특히 이종이식의 가장 큰 문제점인 면역거부반응이 거의 제로에 가까워 면역억제제가 필요없었다.
이같은 임상시험은 올해 6월 미국심장학회 저널인 Circulation, Cardiovasc intervention에 소개됐으며, 일본, 대만, 홍콩 등 아시아 국가 뿐만 아니라 유럽에서도 상용화 문의가 잇따르고 있다.
현재 연구팀은 유럽 허가를 위해 다음 달 유럽 6개국, 11개 소아심장센터와 만나 협의하기로 했고 내년 초부터 임상시험을 시작할 예정이다.
심장에는 혈액순환을 조절하는 판막 4개가 있다. 가장 흔한 판막질환은 대동맥의 판막 협착이다. 그러나 대동맥 인공판막은 이미 미국 등 선진국에서 개발한 타비(TAVI)라는 스텐트-인공심장판막이 상용화되고 있다.
이번 서울대병원 연구팀이 개발한 스텐트 이식 폐동맥 인공판막은 세계 최초로 상용화된 제품으로 그동안 한국과 미국, 중국이 치열하게 경쟁해 왔었다.
현재 외국 제품은 개당 3~4천만 원으로 고가다. 게다가 10년마다 판막을 교체해야 하는데 처음에는 개흉수술을 해야 한다.
하지만 이번 서울대병원에서 개발한 스텐트-폐동맥인공판막은 처음부터 정맥을 통해 시술할 수 있는데다 폐동맥 크기에 맞출 수 있는 유연성도 갖고 있다.
이러한 장점으로 향후 환자의 수술과 경제적 부담의 감소는 물론 수출을 통해 국부 창출에도 기여할 전망이다.
김기범 교수는 "현재 국내 여러 병원에서 추가 임상시험이 진행 중이다. 내년 초부터 유럽 내 허가임상을 진행해 유럽CE인증을 받으면 환자 삶의 질 향상과 한국 의료기술 세계화에 보다 기여할 것"이라고 기대했다.
