[메디칼트리뷴 김준호 기자] 미국과 유럽에서 시판허가를 받은 국내 의약품이 올해 2품목이 추가되면서 지금까지 총 12품목으로 늘어났다.
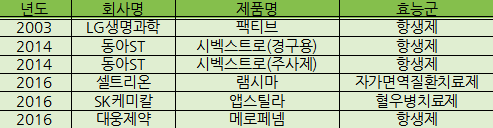
2003년 미국 시장 국내 의약품 승인 1호인 LG생명과학(현 LG화학)의 팩티브 이후 10여년이 지난 2014년부터 동아ST의 시벡스트로 경구제와 주사제, 2016년에는 셀트리온의 바이오시밀러 램시마, SK케미칼의 앱스틸라, 대웅제약의 메로페넴 등이 승인을 받았다.
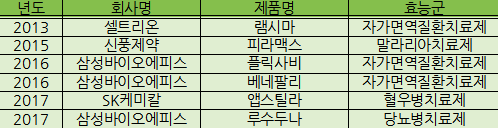
유럽시장 국내 의약품 승인 1호는 2013년 램시마, 이어 2015년에 신풍제약의 피라맥스, 삼성바이오에피스의 바이오시밀러 플릭사바, 2017년 앱스틸라, 삼성바이오에피스의 루수두나가 뒤를 이었다.
미국과 유럽의 시판승인은 없었어도 국내시장에서 연 100억원대 이상의 매출을 올린 토종 블록버스터도 많이 나왔다.
최근 제약업계에 따르면 LG생명과학의 당뇨병치료제 제미글로와 보령제약 고혈압치료제 카나브, 일양약품의 항궤양제 놀텍, 종근당의 당뇨병치료제 듀비에가 연 매출 100억원(2016년 기준)을 돌파했다.
특히 제미글로정은 토종신약 처음으로 520억원의 매출액을 달성했으며, 카나브는 474억원으로 조만간 500억원을 돌파할 것으로 보인다. 놀텍과 듀비에는 각각 225억원과 123억원의 매출을 올렸다.
관련기사
