올해 상반기 제네릭의약품 개발 생물학적동등성시험계획 승인이 총 76건으로 2011년 이후 매년 감소하는 것으로 나타났다.
식품의약품안전처는 24일 시험계획 승인 현황을 분석한 자료에 따르면 2011년 114건, 2012년 108건, 2013년 79건으로 나타났다. 감소 이유는 공동 생동성시험 허용 때문이다.
치료영역별 승인건수는 정신신경계의약품이 25건으로 가장 많았으며 심혈관계의약품(20건), 비뇨생식기계의약품(11건) 순이었다.
스트레스 증가 및 고령화로 인해 관절염치료제, 불안 및 우울장애 등 정신신경계 의약품이 2010년 이후 처음으로 심혈관계 의약품을 제친 것이다.
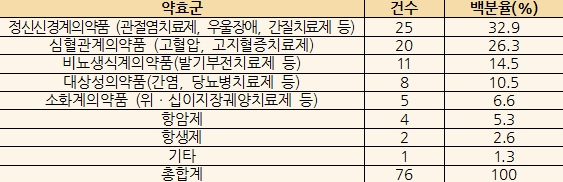
또한 발기부전치료제 등 비뇨생식기계 시험 승인도 11건으로 재작년 3건에 비해 크게 증가해 치료 외에 삶의 질을 높이는 제품의 시장수요를 반영했다.
이번 시험계획 승인의 특징은 단순 제네릭의약품이 아닌 새로운 제형 개발을 위한 시험건수가 작년에 비해 2배 이상 늘어난 점이다.
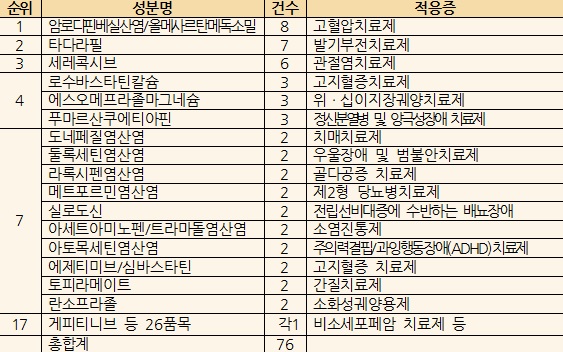
관절염치료제 '세레콕시브'는 제네릭의약품 개발을 위한 승인(6건) 이외에 오리지널 제형인 캡슐제에서 정제로 변경하는 시험 5건을 승인받은 상황이다.
시험 승인 76건 가운데 재심사 또는 특허 만료예정 의약품에 대한 시험이 60건으로 대부분을 차지한 것도 특징이다.
가장 많은 시험계획은 올해 8월에 재심사가 만료되는 고혈압치료제 '암로디핀베실산염/올메사르탄메독소밀'(상품명 세비카)로 8건이었다.
이밖에도 올해 11월 재심사 만료인 '아세트아미노펜/트라마돌염산염'(상품명 울트라셋)은 2건이었다.
내년 9월에 특허만료 예정인 발기부전치료제 '타다라필'(상품명 시알리스)은 7건, 6월에 만료인 관절염치료제 '세레콕시브'(상품명 세레브렉스)는 6건이었다.